
Gázok állapotváltozásai I.
Gázok állapotváltozásai I.
A gázok állapotváltozásai
A gázok állapotát meghatározó mennyiségek
Nyomás (p)
Térfogat (V)
Hőmérséklet (T)
Tömeg (m) vagy anyagmennyiség (n) Ezeket nevezzük állapothatározóknak.
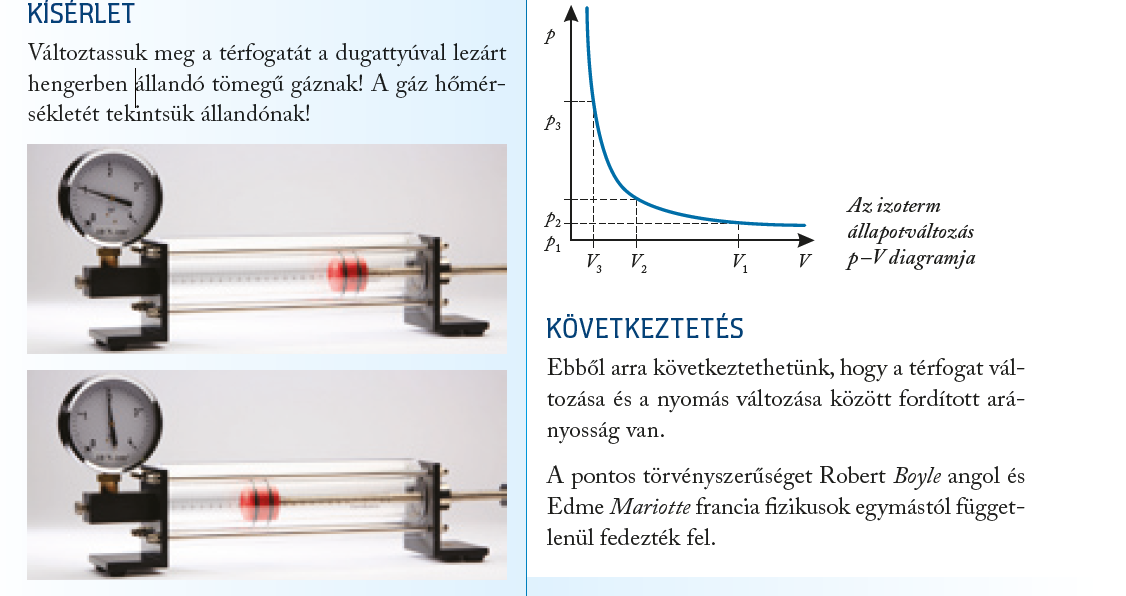
1. Izoterm állapotváltozás (T = állandó)
Jelenség: A hőmérséklet állandó, a térfogat és a nyomás változik.
Törvény: Boyle–Mariotte-törvény
Ha T=állandó
p⋅V=állandó
p1V1=p2V2
Lényege:
Ha csökkentjük a térfogatot → nő a nyomás.
Fordított arányosság.
p–V grafikon: hiperbola.
Forrás: TNK.140.o.
Gyakorlati példa: kerékpárpumpa, Cartesius-búvár.
Pro Cartesius búvár
https://www.youtube.com/watch?v=OomzEqnUSaU
(videó: Tamásné Rudolf)
Izoterm állapotváltozás
Gázok, gáztörvények
Feladatok: 10, 12, 21, 23, 28.
10.
Mi lesz a nyomás, ha a térfogatot nagyon gyorsan felére csökkentjük?
Válasz: C A nyomás a kétszeresnél nagyobbra nő.
Indoklás: Gyors összenyomáskor!!!!! a gáz felmelegszik → nem izoterm → a nyomás a Boyle-törvény szerinti értéknél is nagyobb.
12.
Ideális gázt felére nyomunk össze izoterm és izobár módon. Melyiknél lesz nagyobb a végső hőmérséklet?
Válasz: B Izobár összenyomás végén nagyobb lesz a hőmérséklet.
Indoklás: Izoterm esetben a hőmérséklet nem változik, izobárnál viszont nő.
21.
Igaz-e, hogy p₁V₁ = p₂V₂, ha a kezdeti és végső hőmérséklet azonos?
Válasz: A Csak akkor igaz, ha a folyamat közben is állandó volt a hőmérséklet.
Indoklás: Boyle–Mariotte-törvény csak izoterm folyamatra érvényes, nem elég, hogy a végső T megegyezik a kezdetivel.
23.
Két dugattyú között lévő gáz izoterm állapotban. Ha a jobb dugattyút 10 cm-rel kihúzzuk, mennyit mozdul a bal?
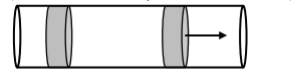
Válasz: B A bal dugattyú kevesebbet mozdul.
Indoklás: A két oldalon lévő gáz térfogata nem egyenlő, ezért a térfogatváltozás aránya sem azonos.
28.
A nyomás megduplázódik, a térfogat 2/3-ra csökken. Lehetséges?
Válasz: C Igen, de csak akkor, ha a hőmérséklet nő.
Indoklás: p·V nem marad állandó → nem izoterm!!!! → a hőmérsékletnek emelkednie kellett.
Izobár állapotváltozás
2. Izobár állapotváltozás (p = állandó)
Jelenség: A nyomás állandó, az állandó tömegű gázok térfogata és kelvinben mért hőmérséklete között egyenes arányosság van.
Törvény: Gay-Lussac I. törvénye
Ha p=állandó
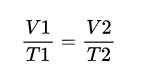
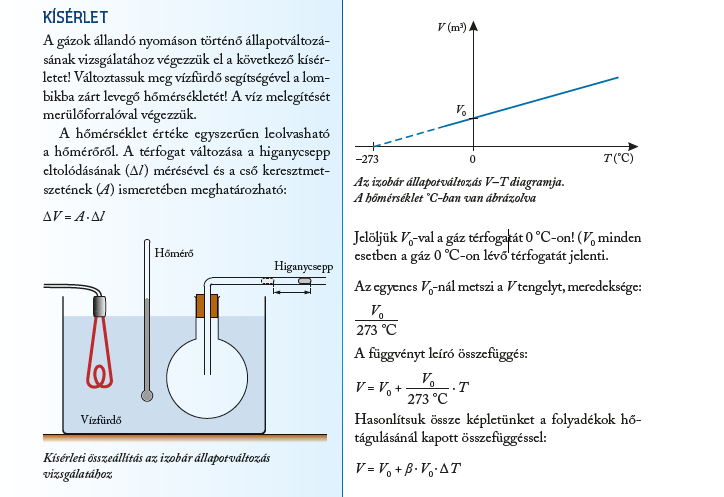
Forrás: TNK.143.o.
Izobár állapotváltozás
Feladatok:
https://kemfiz.hu/fizika_kozep_hotan.html
Feladatok: 9, 11, 18, 25, 30.
9.
20 °C-os héliumot állandó nyomáson 40 °C-ra melegítünk. Hogyan változik a térfogata?
Válasz: C A térfogat nem kétszereződik, csak arányosan nő a kelvin-skálán.
Indoklás: Izobár folyamatban V∼T, de a 20→40 °C nem duplázza meg a kelvinben mért hőmérsékletet.

11.
30 °C-os héliumot 300 °C-ra melegítünk állandó nyomáson. Eléri-e a dugattyú a 20 cm-es éket?
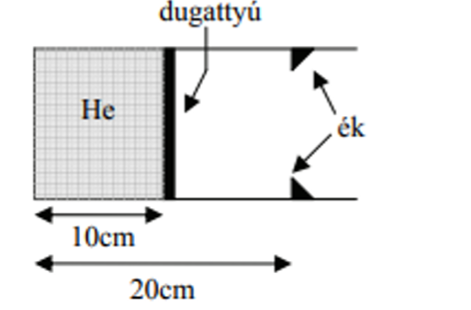
Válasz: B) A dugattyú nem éri el az ékeket a melegítés után sem.
Indoklás: Izobár folyamatban a térfogat a kelvinben mért hőmérséklettel arányosan nő → a hossz kevesebb, mint kétszeresére nő. Nem éri el az éket!

12.
Ideális gázt felére nyomunk össze izoterm és izobár módon. Melyiknél lesz nagyobb a végső hőmérséklet?
Válasz: B Az izobár összenyomás végén nagyobb lesz a hőmérséklet.
Indoklás:
Izoterm összenyomás
Az izoterm szó azt jelenti: állandó hőmérséklet.
Összenyomhatod a gázt, de közben hőt ad le a környezetnek, így a T nem változik.
Izobár összenyomás
Az izobár azt jelenti: állandó nyomás.
Ha a térfogat felére csökken, az ideális gáz törvénye szerint:
T~V
Tehát a hőmérséklet is a felére csökken.
Összegzés
Izotermnél: T ugyanaz marad.
Izobárnál: T csökken.
13.
Adott mennyiségű gáz állandó nyomáson tágul. Mi történik a hőmérséklettel?
Válasz: C A hőmérséklet nő.
Indoklás: Izobár folyamatban V∼T, tehát ha a térfogat nő, a hőmérséklet is nő.
25.
A borosüveg dugóját kifelé húzzuk. Melyik grafikon mutatja a p–V változást?
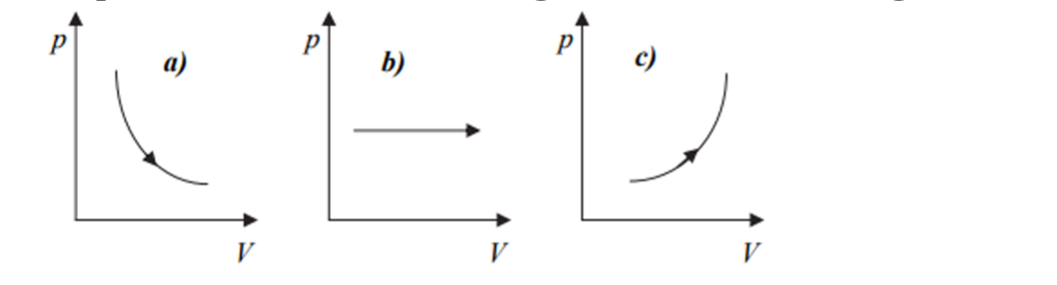
Válasz: A Az "a" grafikon a helyes.
Indoklás: A dugót kifelé húzva a levegő tágul, miközben a külső nyomás gyakorlatilag állandó. A helyes grafikon tehát: A térfogat nő, a nyomás pedig csökken.
30.
Elzárt hélium nyomását és térfogatát több állapotban megmértük. Melyik mérésnél volt a legmagasabb a hőmérséklet?
A) Amikor a térfogata 4 liter, nyomása 0,5 ·10⁵ Pa volt.
B) Amikor a térfogata 3 liter, nyomása 0,75 10⁵ Pa volt.
C) Amikor a térfogata 0,9 liter, nyomása 2 ·105 Pa volt
Válasz: C A 0,9 liter – 2·10⁵ Pa állapotban volt a legmagasabb hőmérséklet.
Indoklás: A hőmérséklet az ideális gáz törvénye szerint a pV szorzattal arányos:
T ~ pV
Számoljuk ki pV-t mindhárom esetben:
A: 0,5⋅4 =2
B: 0,75⋅3=2,25
C: 2⋅0,9=1,8
A legnagyobb érték a B esetben van, tehát ott volt a legmagasabb a hőmérséklet.
