
42. Gázok állapotváltozásai 2.
42. Gázok állapotváltozásai 2.
Izochor állapotváltozás
Adott tömegű gáz:
Térfogat állandó (V = állandó).
Csak nyomás (p) és hőmérséklet (T) változik.
Tapasztalat
Melegítés → nyomás nő
Hűtés → nyomás csökken
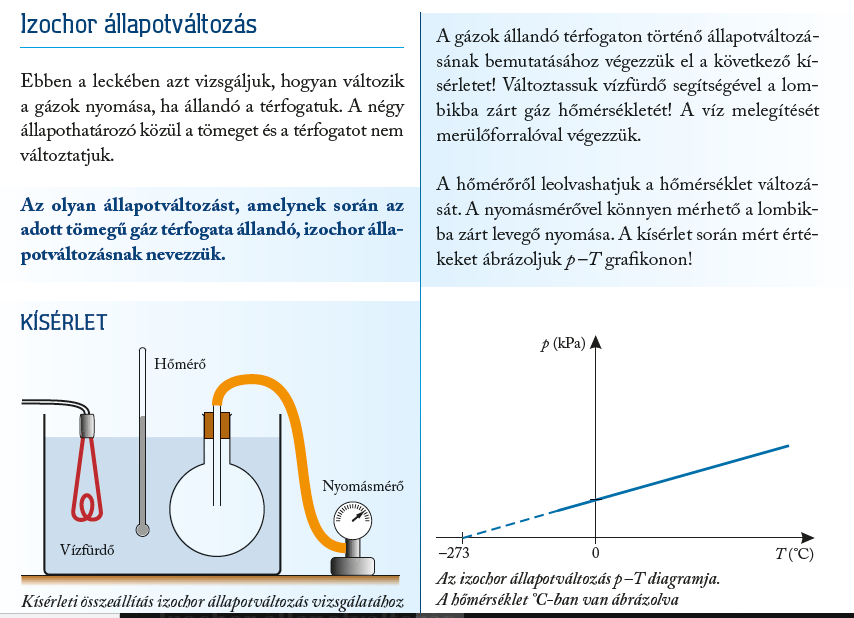
Grafikon
p–T grafikon: egyenes, amely –273 °C-nál metszi a tengelyt.
Kelvin-skálán: egyenes arányosság.
Magyarázat
A részecskék gyorsabban mozognak → nagyobb ütközési erő → nagyobb nyomás.

https://kemfiz.hu/fizika_kozep_hotan.html
14.
Zárt tartályban lévő gázt 100 °C-ról 200 °C-ra melegítünk, a térfogat állandó. Hogyan változik a nyomás?
18.
Egy gázt kétféleképpen melegítünk:
állandó térfogaton a nyomását kétszeresére növeljük,
állandó nyomáson a térfogatát kétszeresére növeljük. Melyikben melegszik jobban?
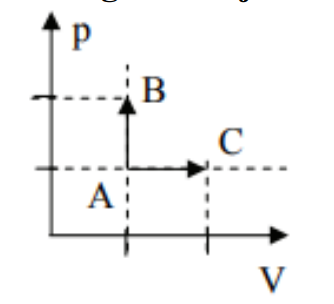
Válasz: C) Ugyanakkora lesz a hőmérséklet mindkét esetben.
Indoklás: Ideális gázra:
eset: V állandó, p kétszeres → T is kétszeres.
eset: p állandó, V kétszeres → T is kétszeres.
Mindkét folyamatban a hőmérséklet ugyanannyiszorosa lesz a kezdetinek, tehát ugyanannyira melegszik fel.
24.
Zárt tartályban lévő nemesgázt melegítünk. Miért nő a nyomás?
Válasz: A) A tartályban lévő atomok lendületének nagysága megnőtt.
Indoklás: A tartály merev, a térfogat állandó (izokór). Melegítéskor a részecskék átlagos sebessége nő, így az ütközések során átadott impulzus (lendületváltozás) is nagyobb. Ez okozza a nyomás növekedését.
29.
Állandó térfogatú tartályban 20 °C-ról 40 °C-ra nő a gáz hőmérséklete. Mekkora lesz a nyomás a végén?
Válasz: B) Kevesebb mint 2⋅105 Pa.
Indoklás:

31.
Állandó térfogatú, lezárt tartályban lévő hélium hőmérséklete 30 °C-ról 10 °C-ra csökken. Mi változik: nyomás, sűrűség?
Válasz: B) Csak a nyomása változik, a sűrűsége nem.
Indoklás: A tartály állandó térfogatú és zárt, tehát a gáz mennyisége és a térfogata is állandó → a sűrűség (ρ=m/V) nem változik. A hőmérséklet csökkenése miatt az ideális gáztörvény szerint a nyomás arányosan csökken.
36.

Adiabatikus állapotváltozás
Lényege
Nincs hőcsere a környezettel (Q = 0).
A folyamat gyors vagy a rendszer hőszigetelt.
Mi történik?
Összenyomás → melegszik a gáz.
Tágulás → hűl a gáz.
Miért?
A gáz belső energiája csak a munkavégzés miatt változik.
Összenyomáskor a környezet munkát végez a gázon → T nő.
Táguláskor a gáz végez munkát → T csökken.
Jellegzetesség
A nyomás gyorsabban nő, mint izotermnél.
A nyomás gyorsabban csökken, mint izoterm tágulásnál.
https://kemfiz.hu/fizika_kozep_hotan.html
10.
A térfogatot nagyon gyorsan felére csökkentjük. Mekkora lesz a nyomás?
Válasz: C A nyomás a kétszeresnél nagyobbra nő.
Indoklás: Gyors összenyomás → adiabatikus → a gáz felmelegszik → a nyomás nagyobb lesz, mint az izoterm kétszeres érték.
19.
Egy hőszigetelt hengerben a dugattyúra plusz tömeget teszünk. Mi változik meg?
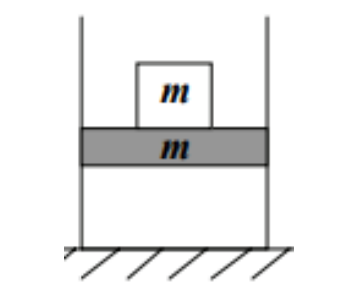
Válasz: B A gáz nyomása és térfogata változik.
Indoklás: A dugattyú lenyomja a gázt → adiabatikus összenyomás → p nő, V csökken, de hőmérséklet csak a munkavégzés miatt változik.
20.
Hőszigetelt hengerben hogyan növelhető a gáz hőmérséklete?
Válasz: C A térfogat csökkentésével.
Indoklás: Adiabatikus összenyomáskor a gáz felmelegszik, mert a környezet munkát végez rajta.
22.
A bal oldali gázt melegítjük, a dugattyú hőszigetelt. Mi történik a jobb oldali gáz hőmérsékletével?
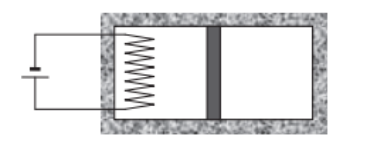
Válasz: A A jobb oldali gáz hőmérséklete nő.
Indoklás: A dugattyú elmozdul → a jobb oldali gáz adiabatikusan összenyomódik → melegszik.
26.
A hengert lassan, óvatosan felállítjuk és visszahelyezzük az asztalra az
ábra szerint.
Hogyan változik a dugattyúnak a henger szájától mért távolsága?
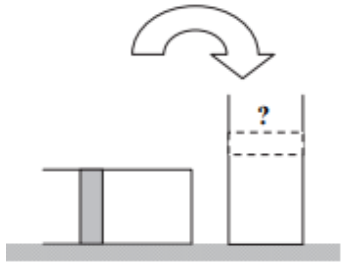
Válasz: A) A távolság megnő, mivel a dugattyú összenyomja a gázt.
Indoklás: A súlypont megváltozik → a dugattyú többlet terhelést kap → adiabatikus összenyomás → kisebb térfogat. A dugattyú lejjebb kerül.
28.
p megduplázódik, V 2/3-ra csökken. Lehetséges?
Válasz: C Igen, ha a hőmérséklet nőtt.
Indoklás: p·V nem marad állandó → nem izoterm → adiabatikus vagy más nem izoterm folyamat → T nő.
